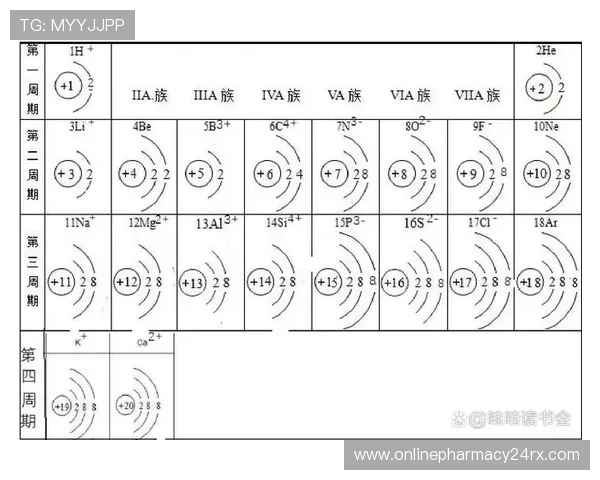
PT电子轨道排布在元素周期表中遵循一定的规律,随着原子序数的增加,电子逐渐填充不同的轨道层次。主要表现为电子配置由内向外逐步扩展,轨道类型由s、p、d、f逐渐丰富。理解这些变化规律,有助于掌握元素的化学性质和反应行为。本文将从电子轨道的基本概念出发,分析元素周期表中PT电子轨道排布的变化规律及其背后的电子配置原理,帮助读者更好理解元素的电子结构演变。
元素的电子轨道主要包括s轨道、p轨道、d轨道和f轨道。它们的填充顺序遵循“能量最低原则”,即电子优先填充能量较低的轨道。根据量子力学的规则,s轨道每层最多容纳2个电子,p轨道最多6个,d轨道最多10个,f轨道最多14个。随着原子序数的增加,电子逐步填充这些轨道,从而形成不同的电子配置。比如,氢和氦主要填充s轨道,碳、氧等元素开始填充p轨道,而过渡元素则涉及d轨道的填充,镧系和锕系元素涉及f轨道的填充。这一规律在元素周期表中表现为周期和族的变化,体现了电子轨道排布的系统性和规律性。
在元素周期表中,每一周期代表电子逐层填充的过程,从左到右,电子逐渐填满s和p轨道,形成不同的电子配置。第一周期只有s轨道,第二和第三周期开始填充s和p轨道,形成主族元素。过渡元素(第4、5、6、7周期)开始填充d轨道,表现为d轨道电子数的增加。镧系和锕系元素则涉及f轨道的填充,表现为f轨道电子数的变化。这些变化规律使得元素的化学性质具有一定的周期性和规律性,电子配置的变化直接影响元素的化学反应性和物理性质。
电子配置的变化直接决定了元素的价电子数,进而影响其化学性质。比如,主族元素的价电子主要在s和p轨道,决定了它们的化合价和反应能力。过渡元素的d轨道电子则影响其多价性和催化性能。镧系和锕系元素的f轨道电子则赋予它们特殊的磁性和光学性质。电子配置的变化规律帮助我们理解元素在化学反应中的行为,比如氧化还原反应、配位能力等都与电子排布密切相关。
元素周期表中的周期性源于电子轨道的逐层填充规律。每当一个新周期开始,电子开始填充新的能级,导致元素性质的周期性变化。族元素具有相似的电子配置,表现出相似的化学性质。比如,碱金属的最外层电子都在s轨道,表现出强还原性;卤素的最外层电子在p轨道,表现出强的氧化性。这种周期性规律使得元素的性质可以通过电子配置的变化进行预测和理解,成为化学学习的重要基础。
PT电子轨道排布在元素周期表中的变化规律体现了电子能级逐步填充的基本原则,随着原子序数的增加,电子逐层填充s、p、d、f轨道,形成不同的电子配置。这些变化规律不仅决定了元素的化学性质,也使得元素周期表具有明显的周期性。理解电子轨道的排布和变化规律,有助于深入掌握元素的电子结构和化学行为,为学习和研究元素的性质提供理论基础。掌握这些规律,是理解元素周期表奥秘的关键所在。最终,电子配置的变化 永利电子手机版会员登录规律贯穿于元素的所有化学性质中,成为化学科学的重要支撑。